科学家利用“时间机器”技术了解干细胞如何制造特定细胞类型的编程方法
通过发现这一过程,研究人员希望他们能够找到新的癌症免疫疗法,并计划将这一技术扩展到其他领域,如发现肿瘤启动的新药物靶点。
研究结果一览:
- WEHI的研究人员开发了一种新的单细胞方法,以了解导致干细胞制造特定细胞类型背后的编程方法。
- 通过在不同的平行测试中测试单个干细胞,研究人员发现了500个预测树突状细胞命运的基因。
- 利用CRISPR筛选,他们在500个编程树突状细胞生产的基因中发现了30个关键基因。
- 研究人员打算扩大使用这一技术,寻找癌症发展中的 "大爆炸 "时刻,以确定新的抗癌药物靶点。
研究“姐妹”细胞
该研究由Shalin Naik博士、Luyi Tian博士、Sara Tomei和Jaring Schreuder领导,并发表在《免疫》杂志上,该研究概述了由激素Flt3配体驱动的树突状细胞生成的启动过程,该配体用于免疫疗法。
研究团队开发了一种新技术,将单个细胞的基因表达与它制造的细胞类型联系起来。
“我们发明了一种名为‘SIS-seq’的技术,以研究从‘母’干细胞平行降生的‘姐妹’细胞,”Naik博士说。“由于RNA测序破坏了单个干细胞,你只能测量细胞的遗传内容,但却失去了知道它本来会制造什么的机会。所以,没有办法再回到过去去寻找这个问题。”
“通过让单个干细胞只分裂几次,而不是全部分裂,我们能够分别对‘姐妹们’进行测试。有的检测它们制造的东西,有的检测它们的基因含量。”
“通过这种方式,我们已经能够将基因与制造的细胞类型联系起来。”
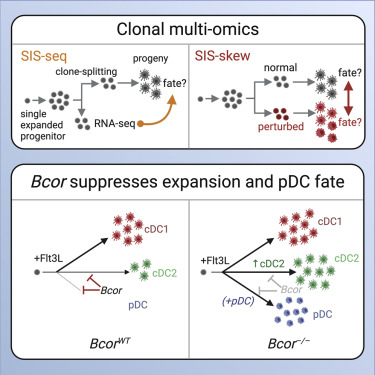
发现30个新基因
Naik博士说,如果没有技术的进步,使团队能够同时回答多个问题,这些发现是不可能的。“利用CRISPR筛选,我们测试了500个预测树突状细胞命运的基因,并发现了30个新基因,这些基因实际上可以编程制造树突状细胞,”他说。
Naik博士说,这一突破可以为新的药物靶点铺平道路,以对抗癌症和改善免疫疗法治疗。“我们现在已经有了一份基因列表,可以尝试在培养皿中生成或促进人类树突状细胞,用于免疫疗法,”他说。“而且我们将扩大这一技术的使用范围,找到对每一种不同的人类免疫细胞类型的生成进行编程的基因。”
寻找癌症启动的“大爆炸”
通过使用这种技术在单细胞水平上检查细胞,研究人员还打算找到癌症发展中的“大爆炸”时刻,以便创造新的药物靶点来抗击癌症和改善免疫疗法。
“利用我们的时间机器技术,我们希望能够确定组织生成中的哪些正常程序被单细胞中的致癌基因所劫持,然后利用这些信息找到新的治疗靶点。”Naik博士说。